三生制药(01530.HK)今日发布2025年度业绩公告。三生制药以创新研发突破与全球化战略合作为双轮核心驱动,交出一份量质齐升的高质量成绩单:全年实现营业收入177.0亿元,首次突破百亿元大关,同比增长94.3%;归母净利润84.8亿元,同比增长305.8%;经调整归母净利润84.5亿元,同比增长264.6%,盈利能力实现跨越式跃升,彰显强劲增长动能。
2025年,公司全年研发费用达15.2亿元,同比增长14.6%,为创新管线推进提供坚实保障。截至2025年末,公司财务资源跃升至204.0亿元,有息负债比率降至9.8%,综合财务成本实现正向贡献达2.3亿元,资产负债结构进一步优化。充沛的现金流与稳健的资本结构为长远发展筑牢资金根基。公司延续稳定的分红政策,派发2025年度股息0.25港币/股,以扎实的股东回报传递长期发展信心。
报告期内,三生制药与辉瑞达成总金额超60亿美元的全球授权合作,获得14亿美元首付款及1亿美元股权合作,创下中国创新药出海首付款最高纪录。核心产品特比澳®新适应症成功获批,三款新药接连获批上市,三款产品进入NDA阶段,构建多领域创新管线矩阵,全球化竞争力与核心治疗领域优势进一步夯实,为公司高质量发展注入强劲动力。
一、与辉瑞达成全球合作,创中国创新药出海纪录
2025年,三生制药全球化战略迎来关键突破,公司与辉瑞就自主研发的PD-1/VEGF双抗SSGJ-707达成全球合作,成为生物医药行业年度标志性事件。
根据合作协议,三生制药授予辉瑞SSGJ-707全球开发与商业化权利,交易总额最高超60亿美元,公司同时享有基于全球累计收入的梯度双位数分成。其中14亿美元首付款及1亿美元股权合作,一举刷新中国创新药单笔出海授权交易的首付款纪录。这一重磅合作不仅获得国际制药巨头对中国创新药研发质量、标准及体系的高度认可,更充分彰显了三生制药乃至中国生物医药创新的全球竞争力。
此次合作中,三生制药保留SSGJ-707在中国及全球临床、商业化产品的供货权利。目前,首批用于全球临床开发的707双抗原液已成功交付,标志着双方合作正式进入实质性执行阶段,全球商业化落地进程全面提速。
依托辉瑞全球顶尖的临床资源,SSGJ-707的全球临床高效推进,已启动9项国际多中心临床试验,覆盖鳞状/非鳞状非小细胞肺癌、转移性结直肠癌、广泛期小细胞肺癌、胃食管结合部癌、转化型小细胞肺癌、局部晚期/转移性肝细胞癌、局部晚期/转移性尿路上皮癌、局部晚期/转移性肾细胞癌等多个高发癌种。未来,还将持续拓展该品种更多适应症及联用治疗方案,充分释放这一核心创新品种的全球临床价值与商业增长空间。
二、创新价值密集兑现,构筑新增长引擎
2025年至2026年初,三生制药迎来产品获批密集收获期,三款新药接连上市、核心产品获批新适应症、商业化产品纳入医保目录和权威指南、多款产品进入NDA阶段,多维创新价值加速转化,为业绩持续增长注入强劲动力。
三款新药接连获批,丰富临床治疗选择
安沐奇塔单抗(益赛拓®):2026年2月获批上市,用于治疗中重度斑块状银屑病。该产品第2周即起效、12周PASI100领先、52周持续清除,无中和抗体、ADA仅 0.7%,感染风险更低;维持期每8周一次的简化给药方案,大幅降低患者年度用药频率,有效减少长期治疗的时间成本与心理压力,显著提升治疗依从性。 罗赛促红素α注射液(新比澳®):2026年3月获批上市,为首个国产长效重组EPO类双周制剂(1类创新药),用于治疗慢性肾病引起的贫血且正在接受促红细胞生成素治疗的血液透析患者。产品拥有120小时超长半衰期、免疫原性低,静脉给药更适合血液透析患者,“两周一次” 的给药方案,大幅降低患者用药频次,显著提升患者治疗依从性,为临床提供更便捷的治疗选择。 艾曲泊帕乙醇胺片:2026年3月获批上市,用于治疗免疫性血小板减少症(ITP)和重型再生障碍性贫血(SAA),为血液疾病患者提供口服用药新选择,进一步完善公司血液疾病领域商业化产品矩阵。
核心产品拓展新适应症,挖掘存量市场增量空间
全球唯一商业化重组人促血小板生成素(特比澳®)于2025年12月获批新适应症,用于计划接受手术(含诊断性操作)的慢性肝病相关血小板减少症(CLDT)患者,为广大围手术期慢性肝病患者提供起效快、疗效稳定、安全性高的升板治疗方案,进一步拓展核心产品的市场覆盖范围。
商业化产品获权威认可,加速临床渗透
紫杉醇口服溶液(柏瑞素®)成功纳入《CSCO胃癌诊疗指南(2025版)》,成为晚期胃癌患者二线治疗的I级推荐(1A 类)方案;该产品也成功纳入2025年国家医保目录。该产品依托创新性脂质自乳化药物递送技术,实现胃癌治疗从 “住院输注” 到 “居家口服” 的模式升级,大幅提升患者用药便利性;目前其复发性或转移性 HER2 阴性乳腺癌适应症NDA已递交并获受理,未来市场空间有望进一步打开。
三款产品进入NDA阶段,后续增长动力充足
613(抗IL-1β单抗):2025年6月急性痛风性关节炎NDA递交并获受理。中国急性痛风市场生物制剂渗透率极低,该产品为国内同类品种中第二家递交上市申请,竞争格局优良,将填补临床未被满足的治疗需求,市场前景广阔。间歇性通风关节炎适应症II期临床推进中。 611(抗IL-4Rα单抗):2026年2月成人中重度特应性皮炎NDA递交并获受理。疗效整体优于达必妥(非头对头对照),支持双周或每四周一次长效给药,疗效更强、依从性更高、长期控制更优;慢性鼻窦炎伴鼻息肉、慢性阻塞性肺气肿、青少年及儿童特应性皮炎等适应症临床推进中,管线潜力持续释放。 601A(抗VEGF单抗):2025年10月视网膜分支静脉阻塞(BRVO)所致黄斑水肿NDA获受理。疗效与雷珠单抗相当,总体安全性和耐受性良好,为眼科临床提供新选择。
三、构建多领域创新管线矩阵,筑牢长远核心竞争优势
2025年,三生制药持续加大研发投入,围绕肿瘤血液科、自身免疫、肾科、皮肤毛发及减重等核心治疗领域,构建起丰富且具有差异化的创新管线矩阵,多款产品处于关键临床阶段,前沿靶点布局领先,为公司长远发展构筑坚实的技术与产品壁垒。
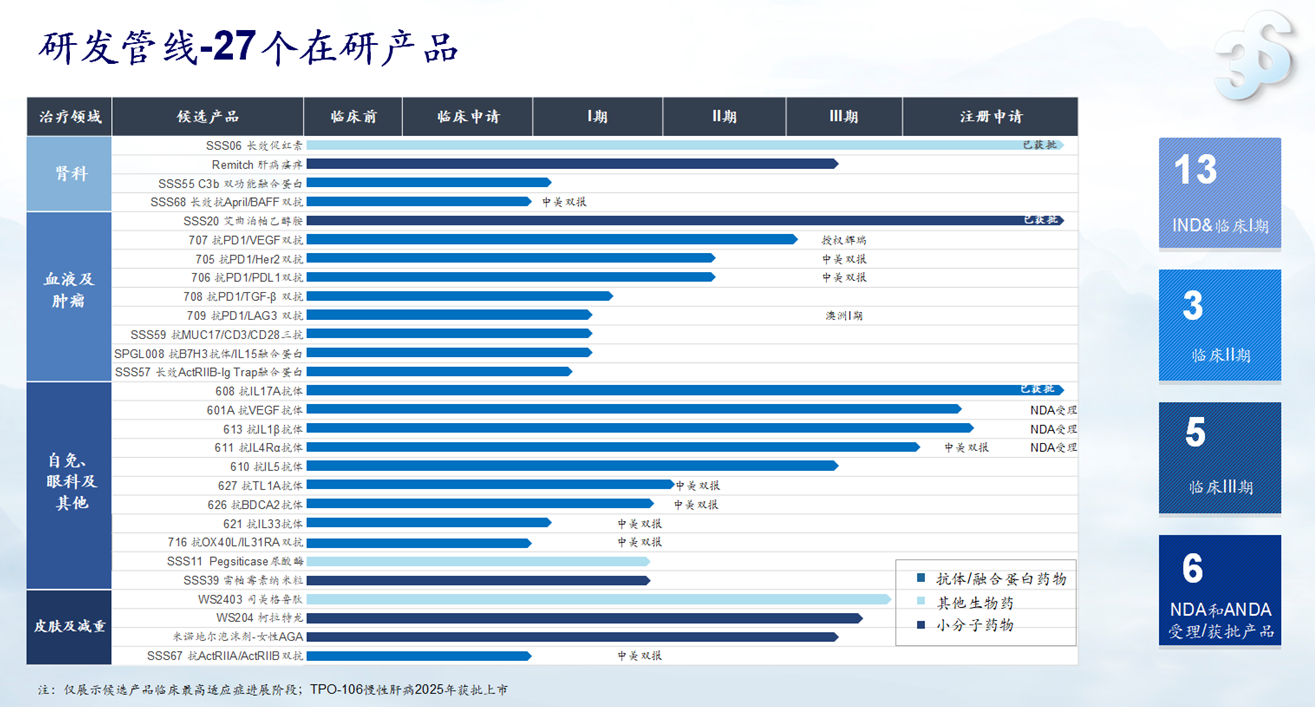
肿瘤血液科:双抗 / 三抗多点布局,打造差异化竞争优势
705(抗PD1/HER2双抗):治疗HER2阳性晚期实体瘤已进入II期临床,为国内唯一积极推进临床的同靶点药物,差异化优势显著。 706(抗PD1/PDL1双抗):治疗晚期非小细胞肺癌、晚期胃肠道肿瘤已进入 II 期临床,覆盖高发瘤种,临床进展顺利。 708(抗PD1/TGFβ双抗)、709(抗PD1/LAG3双抗)、SSS59(抗MUC17/CD3/CD28三抗)、SPGL008(抗B7H3抗体/IL15Rα sushi-IL15融合蛋白)治疗晚期实体瘤,均处于I期临床阶段;SSS57(长效ActRIIB-Ig Trap融合蛋白)治疗MDS相关贫血,处于I期临床阶段。肿瘤血液科管线梯队持续完善,为长期增长储备优质标的。
自身免疫科:多款产品进入关键临床阶段,研发进度国内领先
610(抗IL-5单抗):治疗嗜酸性粒细胞哮喘处于III期临床,研发进度国内第一,有望率先实现商业化。 626(抗BDCA2单抗):治疗系统性红斑狼疮(SLE)已进入Ib期临床,针对自身免疫领域未满足需求。 627(抗TL1A单抗):治疗溃疡性结肠炎(UC)已启动II期临床,布局炎症性肠病核心赛道。 多款早研管线加速推进:包括716(抗OX40L/IL-31RA双抗,治疗AD)、717(CD3/CD19/BCMA,治疗SLE/LN/RA)、718(TL1A/IL-23,治疗IBD)、719(IL-4R/TSLP,治疗哮喘/COPD)、629(IL-23R,治疗银屑病/ IBD)等,全面覆盖自身免疫领域主流与前沿靶点,构建深厚技术护城河。
肾科:聚焦核心需求,前沿靶点布局国内首创
SSS55(C3b双功能融合蛋白):治疗阵发性睡眠性血红蛋白尿症(PNH)、补体相关肾病(CMKD)、牙周炎等适应症,已启动I期临床,为国内唯一积极推进该靶点的企业,填补国内临床空白。 SSS68(长效抗April/BAFF双抗):治疗IgA肾病已获批美国IND,是目前在APRIL/BAFF靶点上唯一进入临床阶段的国产长效双抗,差异化优势显著。
皮肤毛发及减重领域 前瞻布局
WS2403司美格鲁肽减重适应症III期临床试验已完成。 WS204柯拉特龙乳膏剂治疗12岁及以上中重度寻常性痤疮III期临床进行中。 SSS67(抗ActRIIA/ActRIIB双抗)治疗超重/肥胖症已获批美国IND,是国内唯一进入IND申报的创新偏向型双抗,前瞻性布局代谢领域蓝海市场。
三生制药董事局主席兼首席执行官娄竞博士表示:“2025年是‘十四五’规划收官之年,在医保、医疗、医药协同治理下,行业迎来多项标志性变革。商业健康险为创新药打开多元支付通道,中国创新药海外授权屡创佳绩。公司自主研发的SSGJ-707以24%首付比创下出海授权新纪录,彰显中国创新的全球竞争力。2026年,生物医药被列为国家新兴支柱产业,在国家政策推动下,产业正从制药大国向医药强国迈进,公司的创新潜力亦获国际认可。立足三十余年产业积淀,我们坚持守正创新,深耕肿瘤、自免、肾科等领域,加大前沿创新投入,持续优化研发管线,加快推进柏瑞素®、益赛拓®、新比澳®等新品上市推广。在‘让创新生物药触手可及’的使命驱动下,推进更多优质品种早日上市,造福患者。”










发表评论